- Дисциплина: Химия
- Номер вопроса в билете: 21
- Баллы: 1
- Сложность: Базовый
-
Для выполнения этого задания используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
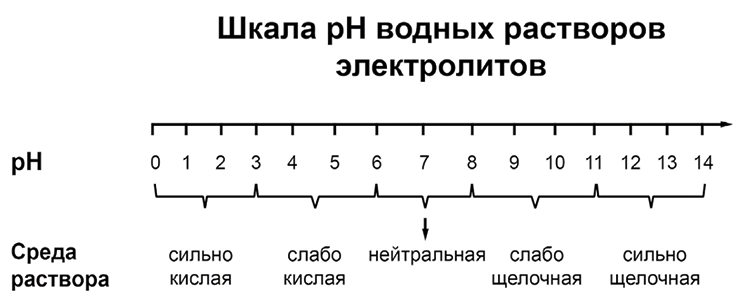
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
- 1) K2S
- 2) Al(NO3)3
- 3) NaF
- 4) HClO3
Баллы: 0 - Подробное решение
K2S — соль образована сильным основанием KOH и слабой кислотой H2S гидролиз по аниону, среда слабощелочная. pH>7
Al(NO3)3 — соль образована слабым основанием Al(OH)3 и сильной кислотой HNO3 гидролиз по катиону, среда слабокислая. pH<7
НClO3 — хлорноватая кислота это сильная одноосновная кислота, среда сильно кислая, pH= 0 -1
NaF — соль образована сильным основанием NaOH и слабой кислотой HF гидролиз по аниону, среда слабо щелочная. pH >7
В порядке возрастания pH:
HClO3 (сильно кислая) - Al(NO3)3 (слабо кислая) - NaF (слабощелочная) K2S (слабощелочная)
Задание крайне плохое. Школьники не могут сравнить среду NaF и K2S. Слабых кислот много, и знать какая из слабых кислот сильнее, или какая слабее наизусть нельзя.
Тут можно написать много формул про степень диссоциации, константу диссоциации, константу гидролиза. Но скажем проще - согласно справочным данным HF более сильная кислота чем H2S. Поэтому диссоциируют по аниону соли более слабой кислоты H2S лучше и среда там чуть более щелочная.
Помоги нам - задонать!